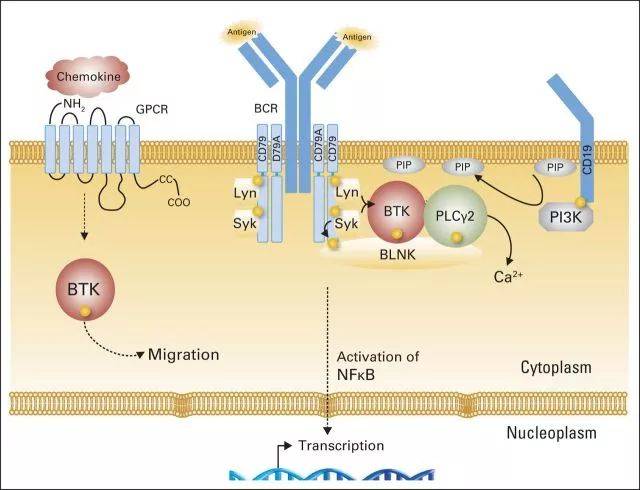
本報訊(記者袁璐)中國新藥研發迎來重大里程碑。今天上午,百濟神州公司宣布,其自主研發的BTK抑制劑澤布替尼通過美國食品藥品監督管理局(FDA)加速批準,用于治療既往接受過至少一項療法的套細胞淋巴瘤(MCL)患者。這標志著,澤布替尼成為迄今為止第一款完全由中國企業自主研發、在FDA獲準上市的抗癌新藥,實現中國原研新藥出海“零的突破”,改寫了中國抗癌藥“只進不出”的尷尬歷史。
記者了解到,在目前已知的淋巴瘤70多個亞型中,套細胞淋巴瘤侵襲性較強,中位生存期僅為三至四年。多數患者在確診時已處于疾病晚期,面臨著治療手段有限、預后不良的困境。而澤布替尼則是一款新型強效BTK抑制劑,目前正作為單藥或與其他療法聯合用藥,在多種淋巴瘤治療中開展臨床試驗。數據顯示,在針對套細胞淋巴瘤的臨床試驗中,84%以上接受澤布替尼治療的患者達到了總體緩解。
長期以來,在我國上市的抗癌原研藥主要依賴進口,而從本土出口海外的藥品則多為原料藥或仿制藥,總體對全球醫藥創新體系的貢獻相對較小。近年,我國醫藥行業加快轉型升級,尤其在藥改、醫改的利好政策驅動下,制藥業興起創新浪潮,大批科學家歸國投入新藥研發,為醫藥產業從仿制轉向創新、從本土走向全球,注入了可持續發展的活力。
澤布替尼誕生于北京昌平的百濟神州研發中心。百濟神州方面透露,澤布替尼獲得FDA批準是基于兩項臨床試驗的有效性數據,其中關鍵性2期臨床研究由北京大學腫瘤醫院牽頭開展。“近年來,我國淋巴瘤的臨床治療和藥物研發步入快速發展的時期。曾經,我們只能期待國外的新藥進入中國,如今情況發生了極大改變。”北京大學腫瘤醫院淋巴瘤科主任朱軍表示,本土自主研發的新藥首次在FDA獲準上市,代表著我國的創新能力和研究水平得到國際上的肯定,為世界提供中國的治療方案。
記者了解到,百濟神州已于2018年8月和10月,向中國國家藥品監督管理局(NMPA)遞交了澤布替尼針對治療復發或難治性套細胞淋巴瘤(MCL)與復發難治性慢性淋巴細胞白血病(CLL)/小淋巴細胞淋巴瘤(SLL)的新藥上市申請,并均被納入優先審評通道,有望早日惠及我國本土患者。在國內獲批后,澤布替尼將在百濟神州位于蘇州桑田島工業園區的小分子藥物生產基地進行商業化生產。
(編輯:鑫果)







 鏡頭下的“電療神壇”:科治好騙局十年未涼,老人帶娃入局背后的情感圍獵
鏡頭下的“電療神壇”:科治好騙局十年未涼,老人帶娃入局背后的情感圍獵 假洋膏藥年銷過億元,平臺監管不能失靈
假洋膏藥年銷過億元,平臺監管不能失靈 AI投資陷阱與維權難,企業如何防范技術合作騙局
AI投資陷阱與維權難,企業如何防范技術合作騙局 “護眼臺燈”亂象調查
“護眼臺燈”亂象調查